COMUNICACIÓN POSTER
AUTORES
Díaz Castela, Manuel; Oliva Nacarino, Pedro; López López, Begona; López Peleteiro, Antia; Suárez Huelga, Celso; Lanero Santos, Marina; Vargas Mendoza, Andrea Katherine; Oterino Durán, Agustin; Llaneza González, Miguel Angel; Villafani Echazú, Walter Javier
CENTROS
Servicio de Neurología. Hospital Universitario Central de Asturias
OBJETIVOS
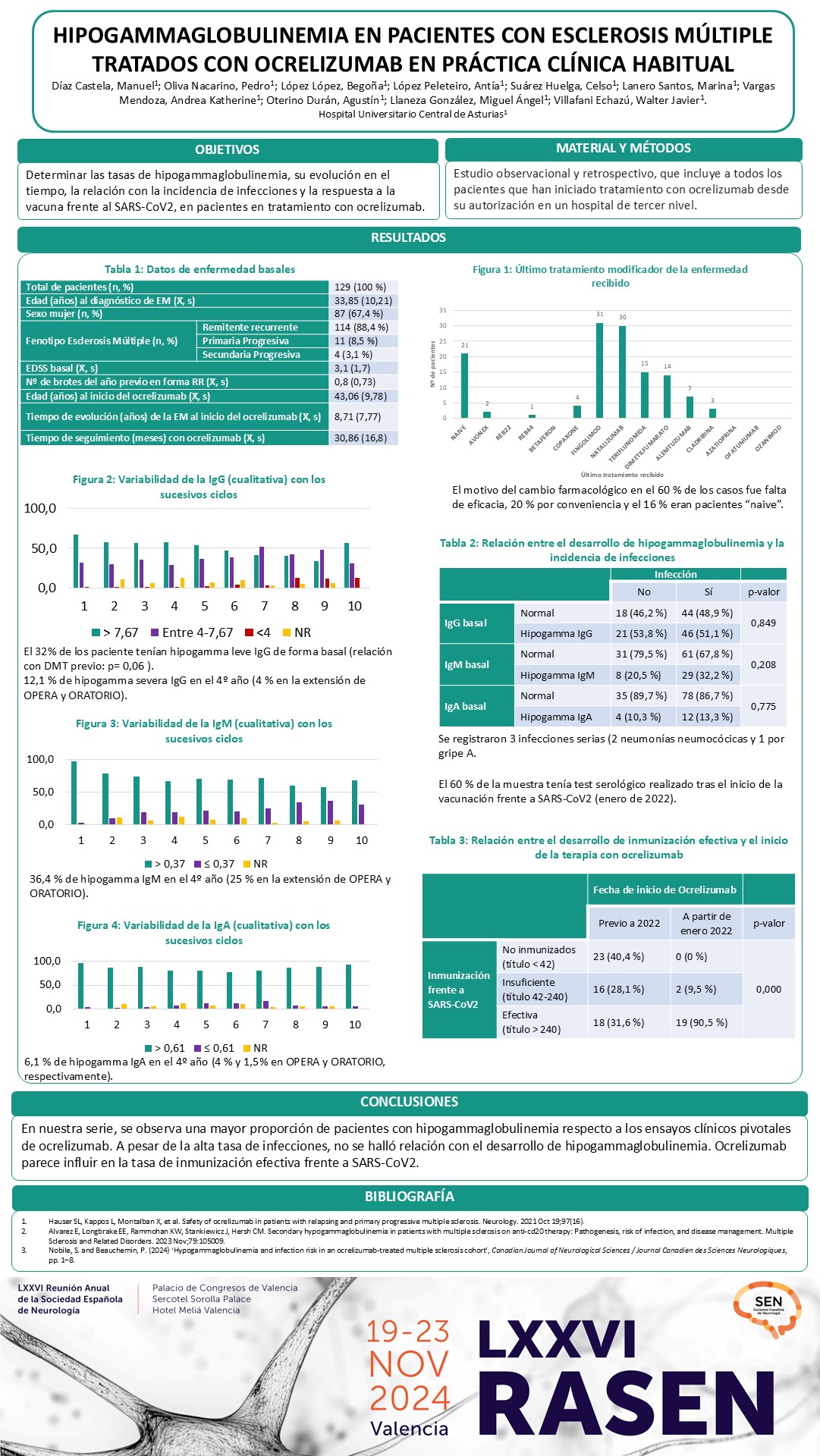
Determinar las tasas de hipogammaglobulinemia, su evolución en el tiempo, la relación con infecciones y la respuesta a la vacuna SARS-CoV2, en pacientes en tratamiento con ocrelizumab.
MATERIAL Y MÉTODOS
Estudio observacional y retrospectivo, que incluye a todos los pacientes que han iniciado tratamiento con ocrelizumab desde su autorización en un hospital de tercer nivel.
RESULTADOS
Se analizan 129 pacientes, incluyendo 87 mujeres (67%), edad media de 46 años, 114 con fenotipo remitente recurrente, con una tasa de brotes en el año previo de 0,8 y EDSS basal 3,1. 21 pacientes eran “naive” y 108 procedían de tratamientos previos. El tiempo medio de tratamiento fue de 30 meses. A los 4 años un 12,1% de pacientes tenían niveles severamente descendidos de IgG, un 36,4% de IgM, y un 6,1% de IgA. 90 pacientes (60,8%) tuvieron algún tipo de infección, 3 fueron neumonías con necesidad de tratamiento hospitalario, sin objetivar relación con el desarrollo de hipogammaglobulinemia. Se testaron niveles de anticuerpos para SARS-CoV2 en 78 pacientes (60,5%), apreciando una mayor tasa de seroconversión en aquellos que iniciaron ocrelizumab tras el inicio de la vacunación (enero 2022), p-valor = 0,04.
CONCLUSIONES
En nuestra serie, se observa una mayor proporción de pacientes con hipogammaglobulinemia respecto a los ensayos clínicos pivotales de ocrelizumab. A pesar de la alta tasa de infecciones, no se halló relación con el desarrollo de hipogammaglobulinemia. Ocrelizumab parece influir en la tasa de inmunización mediante vacunación frente a SARS-CoV2.