COMUNICACIÓN POSTER
AUTORES
García , Eli 1; Salutregui , I. 2; Ziemssen , T. 3; Diaz-Lorente , M. 4; Fuchs , A. 4; Cornelissen , C. 4
CENTROS
1. Departamento Médico. Novartis Farmacéutica; 2. Departamento Médico. Novartis Farmacéutica S.A., España; 3. Servicio de Neurología. Center of Clinical Neuroscience, Karl Gustav Carus University Hospital; 4. Departamento Médico. Novartis Pharma GmbH
OBJETIVOS
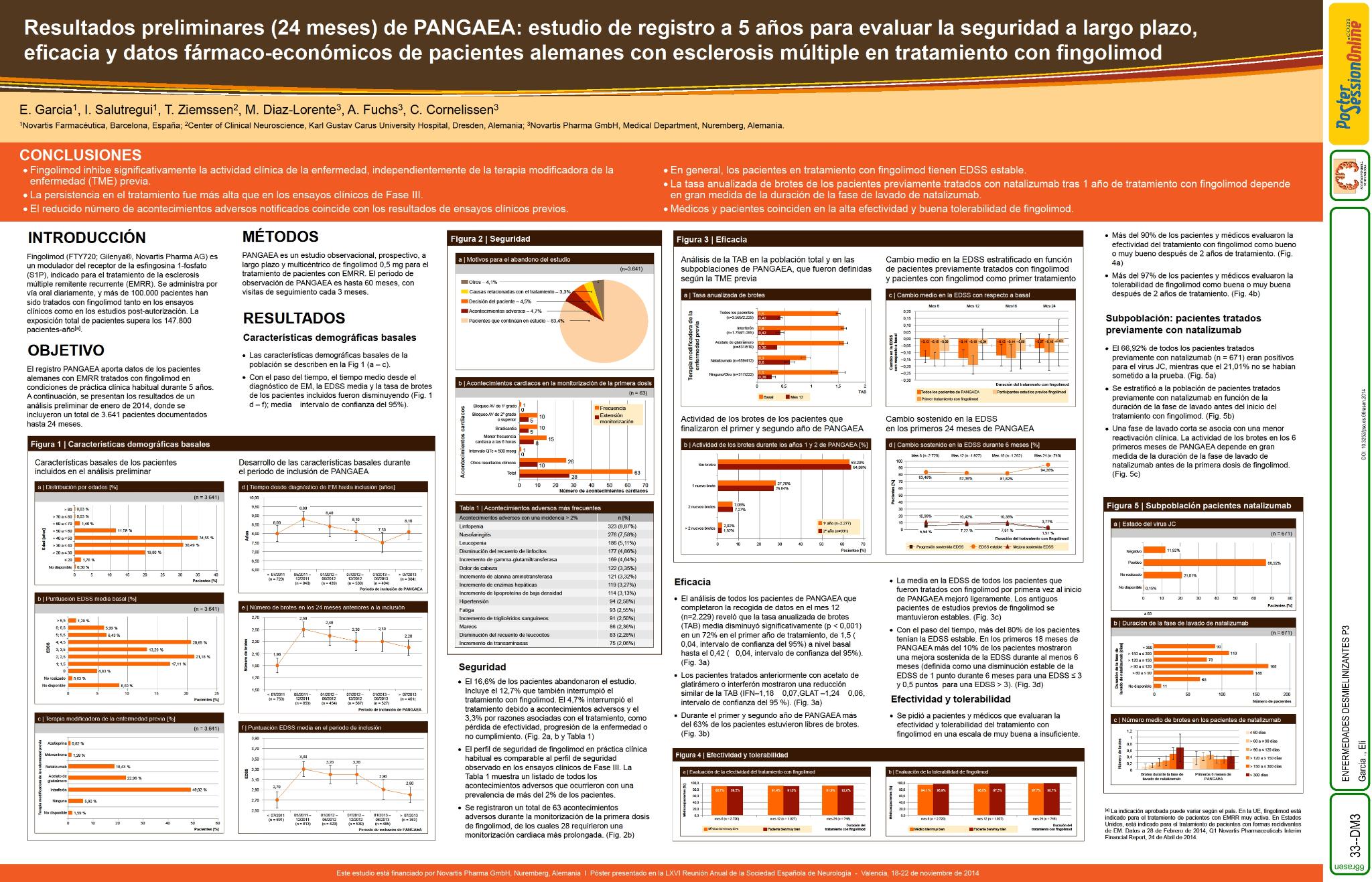
Análisis preliminar a 24 meses de un estudio observacional de 5 años en Alemania que evalúa seguridad, eficacia y datos fármaco-económicos de pacientes con esclerosis múltiple remitente-recurrente (EMRR) tratados con fingolimod en práctica clínica real.
MATERIAL Y MÉTODOS
Además de aspectos de seguridad, eficacia y farmacoeconomía se estimaron aspectos de la vida diaria de los pacientes tratados con fingolimod utilizando cuestionarios: PRIMUS, EQ5-D (calidad de vida), TSQM-9 (satisfacción con el tratamiento), cumplimiento terapéutico y consumo de recursos.
RESULTADOS
A finales de 2013, se reclutaron más de 3900 pacientes en 502 centros. El análisis al mes 18 (n=406) mostró una mejora sostenida en la EDSS en el 16% durante como mínimo seis meses, una progresión en la EDSS en el 10,3% y EDSS estable en el 73,3% durante el primer año de tratamiento. Todos los pacientes mostraron una reducción significativa de la tasa anualizada de brotes (TAB), independientemente de la terapia modificadora de la enfermedad previa (TAB basal/TAB a 12 meses: todos los pacientes 1,5/0,4; pacientes previamente tratados con: IFN1,6/0,4; GLAT:1,6/0,4; natalizumab: 1,1/0,4). Tras 1 año de tratamiento (n=2239), 3,8% pacientes abandonaron el estudio debido a acontecimientos adversos (abandono total del estudio: 11,5%). La TAB de los pacientes previamente tratados con natalizumab tras 1año de tratamiento con fingolimod (n=295), se correlaciona con la duración de la fase de lavado (≤60-≤120días:0,88; >120días:1,19).
CONCLUSIONES
Los resultados preliminares a 24 meses confirman el perfil positivo de seguridad y eficacia de fingolimod, demostrado en los ensayos clínicos Fase III, en condiciones de práctica clínica habitual.