COMUNICACIÓN POSTER
AUTORES
Ciudad Herrera, Antonio 1; Honig , Lawrence S 2; Hake , Ann M 3; Sundell , Karen L 3; Carlson , Christopher D 3; Hoffmann , Vicki Poole 3; Case , Michael G 3; Liu-Seifert , Hong 3; Dean , Robert 3; DeMattos , Ronald 3; Mintun , Mark 4; Khanna , Rashna 3; Selzler , Katie J 3; Siemers , Eric R 3
CENTROS
1. Área Terapéutica de Neurociencias. Lilly; 2. Servicio: Neurological dept.. Columbia University Medical Center; 3. Servicio: Not applicable. Eli Lilly and Company; 4. Servicio: Not applicable. Eli Lilly and Company; Avid
OBJETIVOS
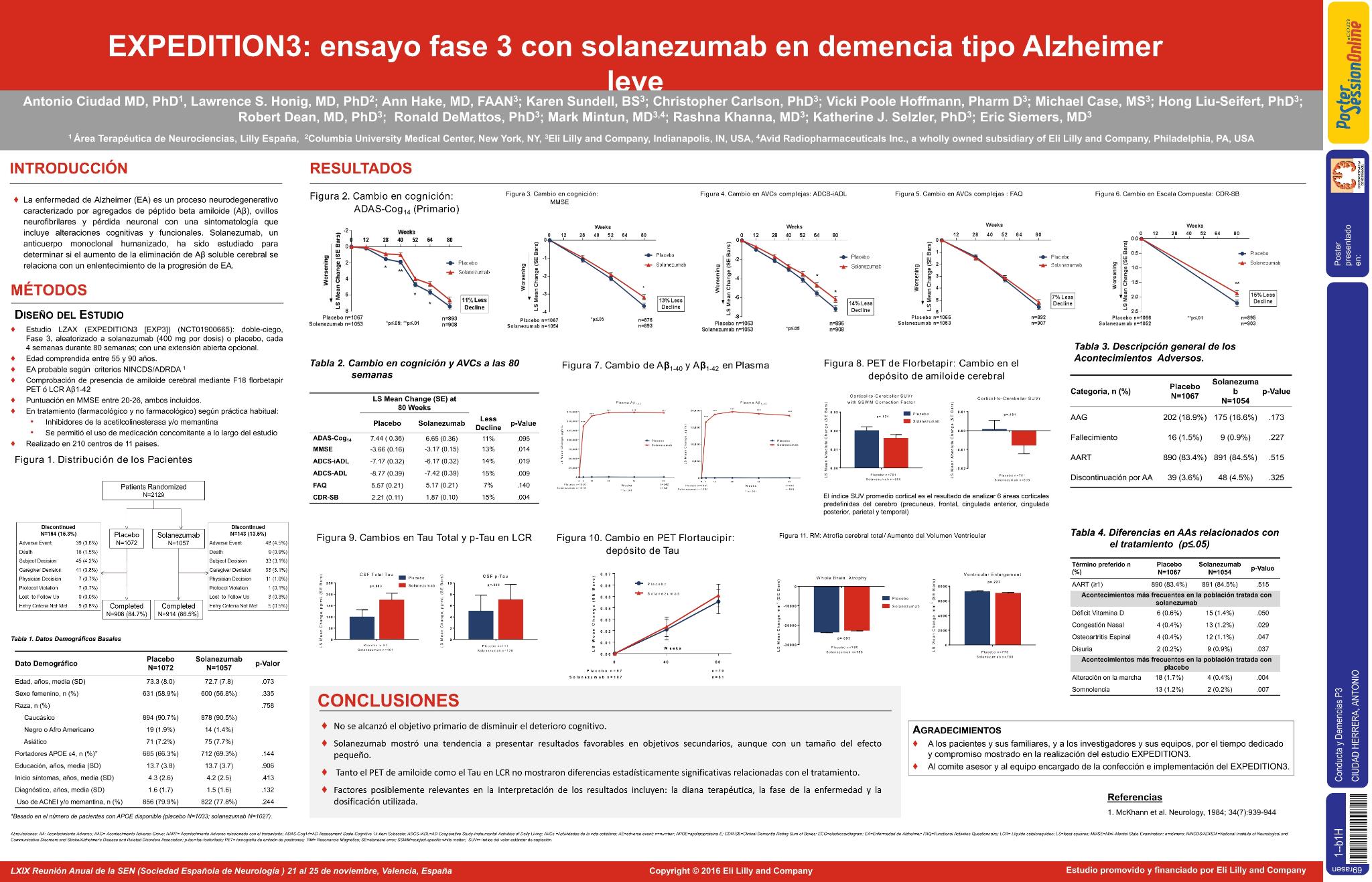
Determinar si el tratamiento con solanezumab ralentiza la progresión de la demencia tipo Alzheimer (DA) leve al aumentar la eliminación de β amiloide soluble cerebral
MATERIAL Y MÉTODOS
Estudio doble ciego, multinacional, fase 3 en pacientes (55-90 años) con AD leve (MMSE: 20-26) con amiloide confirmado mediante biomarcadores. Los pacientes fueron aleatorizados a recibir 400 mg de solanezumab (N = 1057) o placebo (N = 1072). El objetivo primario de eficacia fue el cambio en la puntuación basal-semana 80 en ADS-Cog14 (AD Assessment Scale-Cognitive subscale de 14 ítems)
RESULTADOS
No hubo diferencias estadísticamente significativas entre los grupos de tratamiento en ADAS-Cog14 (p = 0,095); Numéricamente hubo un 11% menos de deterioro cognitivo con solanezumab. Se obtivueron resultados favorables a solanezumab en objetivos secundarios (cognitivos y funcionales) relevantes, MMSE (13% menor deterioro, p = 0,014), CDR-SB (15% menor deterioro, p = 0,004) y ADCS-iADL (14% menor deterioro p = 0,019) pero no en FAQ (7% menor deterioro; P = 0,140). Los pacientes tratados con solanezumab mostraron un aumento estadísticamente significativo en niveles plasmáticos de Aβ1-40 y Aβ1-42 en comparación con placebo ((p<.001 para cada biomarcador)
CONCLUSIONES
En el estudion EXPEDITION3 no se cumplió el objetivo primario de disminuir el deterioro cognitivo. Solanezumab mostró una tendencia a presentar resultados favorables en objetivos secundarios, tanto cognitivos como funcionales, aunque con un tamaño del efecto pequeño. Factores posiblemente relevantes en la interpretación de los resultados incluyen: la diana terapéutica, la fase de la enfermedad y la dosificación utilizada. Solanezumab presentó un perfil de seguridad favorable a la dosis estudiada.