COMUNICACIÓN POSTER
AUTORES
Fuerte Hortigon, Alejandro; null, Rocio; Sánchez Fernández, Felix; null, Julio; null, Sara
CENTROS
Servicio de Neurología. Complejo Hospitalario Regional Virgen Macarena
OBJETIVOS
El uso de Alemtuzumab (ALZ) fue restringido en abril 2019 por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) debido a la aparición de reacciones adversas graves. El objetivo es conocer nuestros pacientes afectados por dichas restricciones y cómo se manejaron
MATERIAL Y MÉTODOS
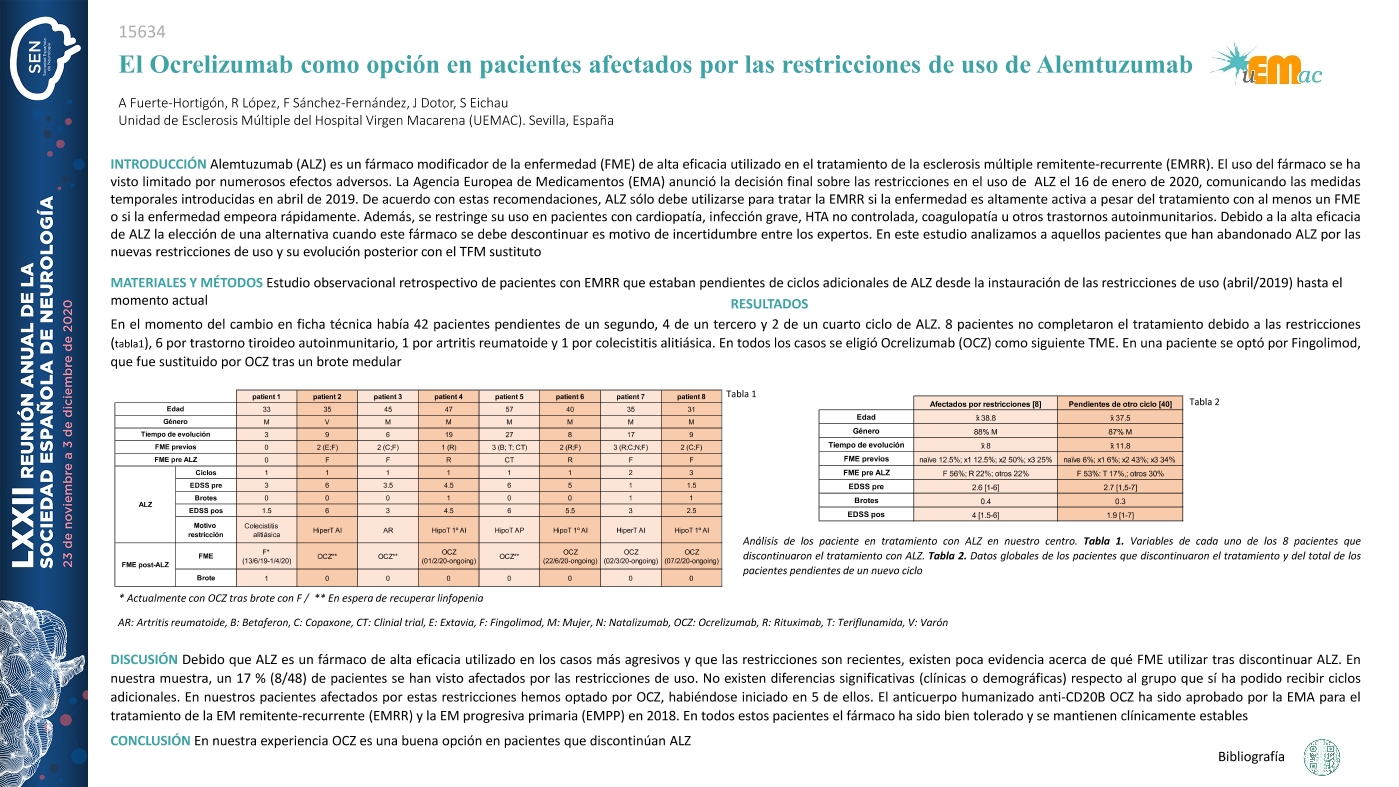
Estudio observacional retrospectivo de pacientes con EMRR que estaban pendientes de ciclos adicionales de ALZ desde la instauración de las restricciones de uso (abril/2019) hasta el momento actual
RESULTADOS
En el momento del cambio en ficha técnica había 42 pacientes pendientes de un segundo, 4 de un tercero y 2 de un cuarto ciclo de ALZ. Edad media 37,5 años, 87% mujeres. Tiempo de evolución medio de EM 11,8 años. EDSS media pre-ALZ 2,74 (1,5-7), post-ALZ de 1,89 (1-7). Número de terapias modificadoras (TME) previas: naïve 6%, x1 6%, x2 43%, x3 34%. TME previa: Fingolimod (F) en el 53% de los casos y Teriflunomida en el 17%, otros 30%. 8 pacientes no completaron el tratamiento debido a las restricciones, 6 por trastorno tiroideo autoinmunitario, 1 por artritis reumatoide y 1 por colecistitis alitiásica. En todos los casos se eligió Ocrelizumab (OCR) como siguiente TME. En una paciente se optó por Fingolimod, que fue sustituido por OCR tras un brote medular
CONCLUSIONES
En nuestra muestra, un 15% de pacientes se han visto afectados por las restricciones de uso. No existen diferencias significativas (clínicas o demográficas) respecto al grupo que sí ha podido recibir ciclos adicionales. Todos los pacientes han recibido OCR tras ALZ con buenos resultados de seguridad y eficacia